Bách khoa toàn thư hé Wikipedia
- Bài này nói tới ete như là 1 trong những lớp công cộng những hợp ý hóa học cơ học. Đối với những nghĩa không giống, coi bài xích Ête (định hướng)

Ete[1] hoặc ête[2] là tên thường gọi công cộng cho 1 lớp hợp ý hóa học cơ học nhập tê liệt với chứa chấp group chức ête — vẹn toàn tử oxy link với nhì (được thay cho thế) group ankyl. Một ví dụ nổi bật là dung môi và dung dịch gây mê điêtyl ête (êthoxyêtan, CH3-CH2-O-CH2-CH3).
Bạn đang xem: ether là gì
Các cấu hình tương tự[sửa | sửa mã nguồn]

Không cần từng hợp ý hóa học với công thức R-O-R' đều là những ête. Ête tránh việc lầm lẫn với những lớp hợp ý hóa học cơ học sau với và một công thức cấu hình tổng quát lác R-O-R'.
- Các hợp ý hóa học vòng thơm tho như furan nhập tê liệt vẹn toàn tử oxy là 1 trong những phần của vòng thơm tho.
- Các hợp ý hóa học nhập tê liệt 1 trong các số những vẹn toàn tử cacbon tiếp tức thì sau vẹn toàn tử oxy được link với oxy, nitơ hoặc lưu huỳnh:
- Các este R-C(=O)-O-R
- Các axêtal R-CH(-O-R)-O-R
- Các aminal R-CH(-NH-R)-O-R
- Các anhyđrit R-C(=O)-O-C(=O)-R
Các ête số 1, bậc nhì, bậc ba[sửa | sửa mã nguồn]
Các thuật ngữ "ête bậc nhất", "ête bậc hai" và "ête bậc ba" đôi lúc được dùng và nó chỉ cho tới vẹn toàn tử cacbon tức thì sau vẹn toàn tử oxy của ête. Trong ête bậc nhất thì vẹn toàn tử cacbon này chỉ được nối với 1 vẹn toàn tử cacbon không giống, như nhập điêtyl ête CH3-CH2-O-CH2-CH3. Ví dụ về ête bậc hai là điisoprôpyl ête (CH3)2CH-O-CH(CH3)2 và ví dụ về ête bậc ba là đi-tert-butyl ête (CH3)3C-O-C(CH3)3.
![]()
![]()
![]()
![]()
Đimêtyl ête, ête bậc nhất, ête bậc hai và ête bậc ba.
Các polyête[sửa | sửa mã nguồn]
Polyête là những hợp ý hóa học với nhiều hơn thế một group ête. Trong khi thuật ngữ này rằng công cộng nhằm chỉ cho tới những polyme như polyêtylen glycol và polyprôpylen glycol, những hợp ý hóa học thấp phân tử giống như những ete lon đôi lúc cũng rất có thể được gọi như vậy.
Tổng hợp[sửa | sửa mã nguồn]
- R-OH + R-OH → R-O-R + H2O
- Phản ứng thẳng này cần thiết những ĐK mạnh (nhiệt và xúc tác acid) và thường thì ko được vận dụng nhập thực tiễn. Các ĐK như vậy rất có thể phá huỷ bỏ những cấu hình mẫn cảm của một trong những group chức. Tồn bên trên một trong những cách thức nhẹ dịu rộng lớn nhằm phát hành ête.
- R-O- + R-X → R-O-R + X-
- Phản ứng này gọi là tổ hợp ête Williamson. Nó bao hàm việc xử lý rượu gốc với những base mạnh muốn tạo rời khỏi anion ankoxide, tiếp theo sau là thêm 1 lượng vừa vặn đầy đủ hợp ý hóa học phệ chứa chấp group thế tương thích (R-X). Các group thế tương thích (X) bao hàm iodide, bromide hoặc sulfonat. Phương pháp này chỉ cho tới thành quả cực tốt so với những vẹn toàn tử cacbon số 1, bởi những vẹn toàn tử cacbon bậc nhì tiếp tục nhập cuộc phản xạ khử E2 khi xúc tiếp với những anion ankoxide gốc dùng nhập phản xạ. Các ête gốc aryl rất có thể được pha trộn theo dõi phản xạ tổ hợp ête Ullmann.
- R2C=CR2 + R-OH → R2CH-C(-O-R)-R2 (xúc tác acid)
Tính hóa học hoá học[sửa | sửa mã nguồn]

Ête là những hợp ý hóa học với phản ứng chất hóa học cực kỳ kém. Chúng chỉ bị thủy phân trong mỗi ĐK cực mạnh ví dụ điển hình nhen lạnh lẽo với BF3 hoặc hâm sôi nhập HBr. Các acid vô sinh chứa chấp halôgen thấp phân tử không giống, ví dụ điển hình HCl cũng tiếp tục phân tách hạn chế những ête, tuy nhiên cực kỳ chậm trễ. Chỉ với HBr và HI là rất có thể phân tách hạn chế bọn chúng với vận tốc nhận ra được.
Các ête rất có thể phản xạ như thể những base Lewis. Ví dụ, điêtyl ête dẫn đến phức hóa học với những hợp ý hóa học của bo, ví dụ như triflorua bo điêtyl êterat F3B:O(CH2CH3)2.
Các êpoxide, hoặc những ête vòng trong những vòng tía member, là rất đơn giản bị tổn hại trước những tiến công loại ái lực phân tử nhân (nucleophil) và bọn chúng phản xạ Theo phong cách này.
Xem thêm: smile nghĩa là gì
Các ête số 1 và bậc nhì với group CH tức thì sau vẹn toàn tử oxy của ête đơn giản và dễ dàng dẫn đến những peroxide cơ học với năng lực khiến cho nổ cao (ví dụ điêtyl ête peroxide) khi xuất hiện oxy, độ sáng và sắt kẽm kim loại cũng giống như những tạp hóa học alđêhít). Vì nguyên nhân này những ête như điêtyl ête và THF thường thì tránh việc dùng thực hiện dung môi trong những tiến độ công nghiệp.
Ete rất có thể được sử dụng thực hiện nhiên liệu
R-O-R’ + O2 -> CO2 + H2O
Điều này cần thiết vì thế những vùng/quốc gia với nhiệt độ rét mướt như Alaska(Hoa Kỳ) hoặc Nga, Canada, hoặc những bang kể từ Washington cho tới Maine( Hoa Kỳ) thông thường xuyên với sức nóng phỏng thấp nhập ngày đông.
Ether rất có thể được khử trở thành hydrocarbon:
Xem thêm: tàu tiếng anh là gì
R – O – R’ + 2H2 -> R-H + R’-H + H2O (to, p, xúc tác Mo-Ni hoặc Co-Mo bên trên nền γ-alumina)
Thuộc tính vật lý[sửa | sửa mã nguồn]
Các phân tử ête ko thể dẫn đến những link hiđrô cùng nhau, vì vậy thành quả là bọn chúng với điểm sôi kha khá thấp khi đối chiếu với những ancol tương tự động. Các ête là ko ưa nước rất là nhiều đối với những este hoặc amit với cấu hình tương tự động.
Danh pháp[sửa | sửa mã nguồn]
Trong khối hệ thống danh pháp IUPAC, những ête được mệnh danh theo dõi cách thức công cộng "ank-oxy-ankan", ví dụ CH3-CH2-O-CH3 là mêtoxyêtan. Nếu ête là 1 trong những phần của những phân tử phức tạp hơn nữa thì nó được mô tả như thể gốc thay cho thế ankoxy, vì vậy -OCH3 rất có thể coi như thể group "mêtoxy-". Tên gọi loại nhì group ankyl và chèn tăng "ête", ví dụ "êtyl mêtyl ête" nhập ví dụ bên trên trên đây, là cơ hội gọi thường thì.
Các ête quan tiền trọng[sửa | sửa mã nguồn]
- Êtylen oxide (epoxide), là ête vòng nhỏ nhất:

- Đimêtyl ête, hóa học đẩy trong những bình xịt:

- Điêtyl ête, một dung môi thông thườn với điểm sôi thấp:

- Đimêtoxyêtan, dung môi với điểm sôi cao:

- Điôxan, ête vòng với điểm sôi cao:

- THF, một ête vòng, một trong những ête phân cực kỳ đơn giản và giản dị nhất được dùng thực hiện dung môi:

- Anisol (mêtoxybenzen), bộ phận chủ yếu của tinh chất dầu hồi:

- Các ête vòng hoa (crown), những polyête vòng được dùng như thể những hóa học xúc tác trả pha:
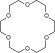
- Polyêtylen glycol, polyête trực tiếp, được dùng nhập mỹ phẩm:

Tham khảo[sửa | sửa mã nguồn]
- ^ Hoàng Phê, Từ điển Tiếng Việt, Viện Ngôn ngữ học tập Việt Nam
- ^ Nguyễn Như Ý, Từ điển Tiếng Việt, Trung tâm Ngôn ngữ và Văn hóa Việt Nam
Xem thêm[sửa | sửa mã nguồn]
- Nhóm chức
- Mêtoxy
- Xăng ête, ko cần là ête nhưng mà là láo hợp ý những ankan với điểm sôi thấp.
- Thiôête, những hợp ý hóa học tương tự động của ête nhập tê liệt vẹn toàn tử oxy được thay cho thế vì chưng vẹn toàn tử sulfur.
Liên kết ngoài[sửa | sửa mã nguồn]
- Ether (chemical compound) bên trên Encyclopædia Britannica (tiếng Anh)
- Trang trang web của ILPI về những ête.









Bình luận